iTAP法について
iTAPとは
iTAP(intelligent Targeted Antibody Phototherapy) は、従来のイムノトキシンに光線力学療法(PDT: Photodynamic Therapy)の概念を統合し、エンドソーム脱出(endosomal escape)を飛躍的に増強させることができる次世代型プラットフォームです。これにより、細胞質到達率が向上し、低用量でも高い薬理効果を発揮することが可能となります。結果として、副作用リスクの低減と治療対象の拡大が期待できます。
iTAPの設計思想
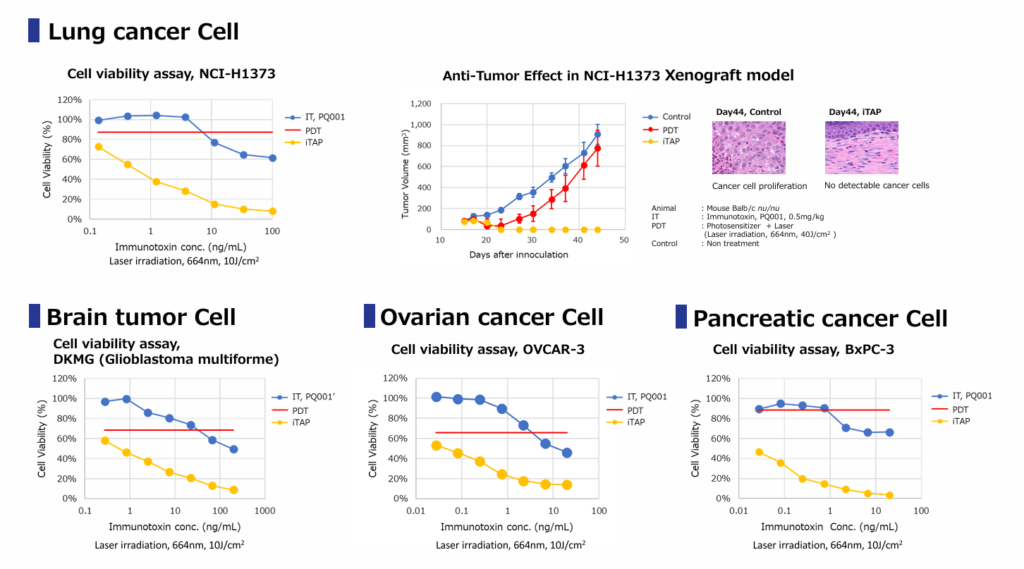
- 高いターゲティング:抗体×サポリンの選択性で標的細胞に集積し、
- 局所・時間選択的なトリガー:PDTを応用したレーザー光による刺激により、標的細胞内でエンドソーム脱出を促進、
- 低用量での薬効発現:細胞質到達効率の向上により、必要投与量の低減と副作用シグナルの抑制を両立します。
iTAP法の適用可能性は広く、標的発現が中~低レベルの固形腫瘍や、細胞内移行が律速であった難治性腫瘍にも展開可能性があります。
iTAPのメカニズム
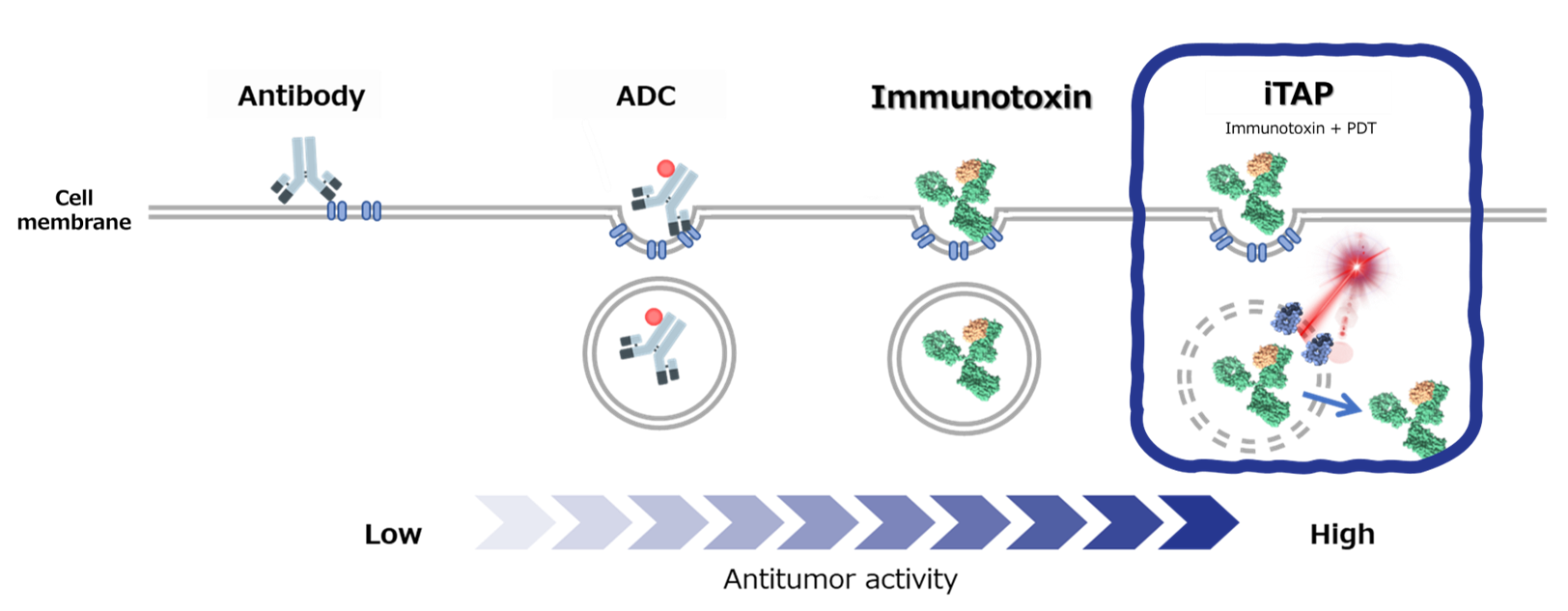
iTAP法は、イムノトキシンが細胞に取り込まれた後に生じる エンドソーム滞留(endosomal trapping)の律速を標的とし、細胞質への移行効率(endosomal escape)を選択的に増強することで、サポリンの細胞障害活性を最大化する技術です。
イムノトキシンは標的抗原に結合し、受容体介在性エンドサイトーシスにより細胞内に取り込まれます。しかし、従来型イムノトキシンの大部分はエンドソーム内に留まり、リソソームに送られて分解されるため、細胞質に到達できる分子はごく一部に限られ、薬理効果が頭打ちになるという根本的な課題がありました。
iTAP は、このプロセスに 光刺激を活用したPDT法の技術を利用することにより、標的細胞内でエンドソーム膜が効率的に破壊されるように設計されています。これにより、イムノトキシンと結合したサポリンが 効率的に細胞質へ移行し、より低用量で高い細胞障害効果をもたらすことが可能となります。
また、このエンドソーム脱出強化は、標的に依存しない“細胞内輸送の改善”であるため、標的発現量が低い腫瘍や、細胞内取り込み自体はできても効果が不十分だった難治性腫瘍などに対しても適用可能性を広げる要因となります。
※PDT(Photodynamic Therapy)について
光線力学療法(PDT)は、光感受性物質(photosensitizer)に特定波長の光を照射し、酸素と反応させて活性酸素種(ROS)を発生させ、標的細胞を選択的に死滅させる治療法です。光感受性物質は腫瘍などの異常組織に集積しやすく、光照射範囲が限定されるため、標的選択性が高いことが特徴です。
PDT はすでに がん(皮膚・頭頸部・肺・膀胱など)や前がん病変(例:日光角化症) を中心に臨床応用されており、安全性と治療効果に関するエビデンスが蓄積された実績ある治療法です。PhotoQ3 は、この 実績ある PDT の技術概念を、細胞内輸送を強化する目的で iTAPに活用しております。



